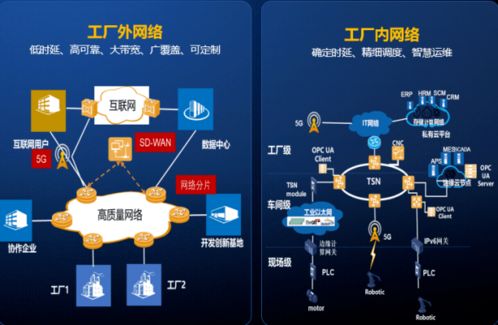
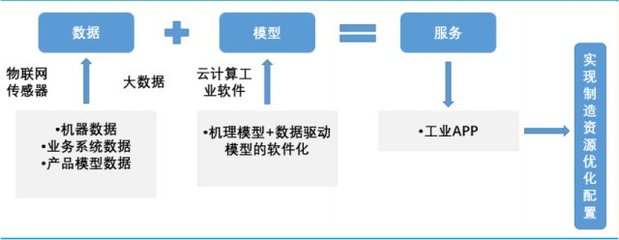
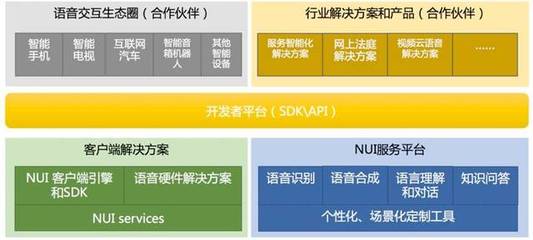
风险评估在制药厂房GMP设计审核与互联网开发应用的融合实例
在高度规范化的制药行业,良好的厂房设施是保障药品质量、安全与有效性的基石。其中,基于《药品生产质量管理规范》(GMP)的设计审核至关重要。与此互联网技术的飞速发展为传统行业带来了新的工具与视角。本文将结合具体实例,探讨风险评估如何作为核心方法论,在制药厂房设施的GMP设计审核与互联网开发及应用之间架起桥梁,实现质量与效率的双重提升。
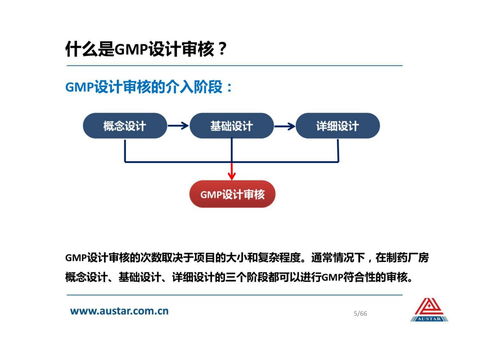
一、 GMP设计审核中的传统风险评估实例
在制药厂房设计阶段,GMP审核的核心是前瞻性地识别、评估并控制可能影响产品质量、患者安全及数据完整性的风险。一个典型实例如下:
实例:生物制品生产车间人流物流交叉风险控制
- 风险识别:在初期图纸审核中,审核团队发现原设计方案中,生产区人员通道与物料传递通道在缓冲间区域存在短暂交汇点,未实现完全物理隔离。
- 风险分析与评估:
- 可能性:尽管有管理程序,但日常操作中人员与物料(特别是外包装)发生交叉的概率被评估为“中等”。
- 严重性:若带入污染或混淆,可能导致产品微生物污染或交叉污染,对患者健康构成严重威胁,严重性为“高”。
- 风险等级:综合评定为“高风险”。
- 风险控制:审核团队建议并最终落实了设计变更:
- 重新规划布局,将人流与物流通道彻底分离,形成单向流。
- 在物料入口设置独立的拆包间和净化传递窗。
- 增加物理隔断和明确的标识系统。
- 风险沟通与审核:此风险评估报告成为设计审核会议的核心文件,促使设计方、建设方与业主达成共识,从硬件源头上降低了污染风险。
二、 互联网开发与应用赋能风险评估与GMP审核
互联网技术并非取代传统的GMP原则,而是通过数字化工具,使其执行得更高效、更精准、更可追溯。
实例:基于BIM与云平台的协同设计与风险动态管理
- 应用背景:在某大型创新药厂房的建设项目中,项目团队引入了建筑信息模型(BIM)技术和基于云的协同管理平台。
- 互联网应用流程:
- 三维可视化设计审核:将传统的二维图纸转化为包含管道、电气、暖通、设备空间关系的三维BIM模型。审核人员可以在虚拟模型中“漫游”,直观地发现诸如管道间距不足、检修空间不够、气流组织不合理等潜在风险点,其识别效率和准确性远高于阅读二维图纸。
- 风险数据库云端联动:平台内置了符合GMP法规和行业指南的风险评估数据库(如ISPE基准指南)。当在模型中标记一个潜在风险点(如洁净室墙面材质接缝处理)时,系统可以自动关联相关的法规条款、历史案例及推荐控制措施。
- 协同评审与追溯:所有设计方、审核专家、业主代表可在同一云端模型上进行标注、评论和审批。每一次风险提出、评估、控制措施讨论、决策的闭环都完整记录在云端,形成可追溯的电子审核追踪,完全符合数据完整性(ALCOA+)原则。
- 移动化现场审核:施工阶段,现场工程师可通过平板电脑访问最新BIM模型,对比实际施工与设计的一致性,实时上传偏差照片并触发风险评估流程,确保施工质量实时受控。
- 价值体现:
- 效率提升:将设计审核周期缩短约30%,并大幅减少施工阶段的返工。
- 质量提升:通过可视化与数据关联,发现了更多隐蔽的、跨专业交叉的风险。
- 知识沉淀:整个项目的风险评估数据形成结构化的知识库,为未来项目提供宝贵参考。
三、 融合展望:构建智能化的厂房设施全生命周期风险管理生态系统
未来的趋势将是更深度的融合。例如,利用物联网(IoT)技术,在厂房设施运行阶段,实时采集环境温湿度、压差、设备运行状态等数据,并输入基于人工智能(AI)的风险预测模型。系统可以预测高效过滤器何时可能失效、设备故障对生产工艺的潜在影响,从而将风险管理从“事后响应”和“定期审核”转变为“事前预警”和“动态调控”。
结论
风险评估是贯穿制药厂房设施从设计、建造到运行全生命周期的灵魂。传统的GMP设计审核为其提供了坚实的法规和科学基础,而互联网开发及应用(如BIM、云计算、物联网)则提供了强大的技术引擎。通过将严谨的质量风险管理理念与先进的数字化工具相结合,制药企业不仅能够更有效地满足法规符合性要求,更能主动构筑起更可靠、更智能、更高效的质量保障体系,最终确保为患者提供安全有效的药品。
如若转载,请注明出处:http://www.hxruanjian.com/product/53.html
更新时间:2026-04-15 14:35:24